3 spannende Wege, wie Chemiker dieses Jahr Verbindungen hergestellt haben
von Bethany Halford
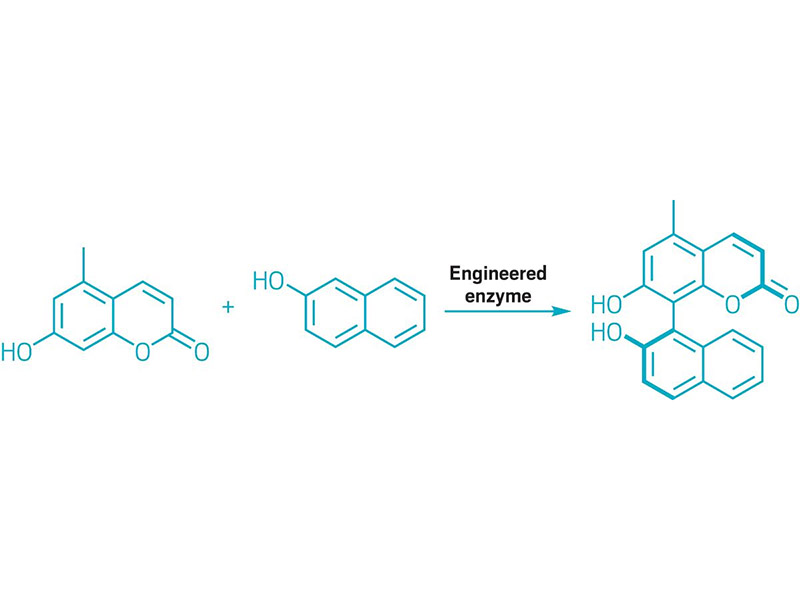
Evolvierte Enzyme bauten Biarylbindungen auf
Schema einer enzymkatalysierten Biarylkupplung.
Chemiker verwenden Biarylmoleküle, die aus über eine Einfachbindung verknüpften Arylgruppen bestehen, als chirale Liganden, Materialbausteine und Pharmazeutika. Die Synthese des Biarylmotivs mittels metallkatalysierter Reaktionen wie Suzuki- und Negishi-Kreuzkupplungen erfordert jedoch typischerweise mehrere Syntheseschritte zur Herstellung der Kupplungspartner. Zudem stoßen diese metallkatalysierten Reaktionen bei der Synthese sperriger Biaryle an ihre Grenzen. Inspiriert von der Fähigkeit von Enzymen, Reaktionen zu katalysieren, nutzte ein Team um Alison R. H. Narayan von der University of Michigan gerichtete Evolution, um ein Cytochrom-P450-Enzym zu entwickeln, das Biarylmoleküle durch oxidative Kupplung aromatischer Kohlenstoff-Wasserstoff-Bindungen synthetisiert. Das Enzym verknüpft aromatische Moleküle zu einem Stereoisomer um eine Bindung mit eingeschränkter Drehbarkeit (siehe Abbildung). Die Forscher glauben, dass dieser biokatalytische Ansatz zu einer Standardmethode für die Herstellung von Biarylbindungen werden könnte (Nature 2022, DOI: 10.1038/s41586-021-04365-7).

Das Rezept für tertiäre Amine benötigte etwas Salz.
Das Schema zeigt eine Reaktion, bei der tertiäre Amine aus sekundären Aminen hergestellt werden.
Die Mischung von elektronenhungrigen Metallkatalysatoren mit elektronenreichen Aminen führt üblicherweise zur Inaktivierung der Katalysatoren. Daher können Metallreagenzien nicht zur Synthese tertiärer Amine aus sekundären Aminen verwendet werden. M. Christina White und ihre Kollegen an der University of Illinois Urbana-Champaign erkannten jedoch, dass sie dieses Problem umgehen konnten, indem sie ihrer Reaktionsmischung eine Art „Salz“ hinzufügten. Durch die Umwandlung sekundärer Amine in Ammoniumsalze konnten die Chemiker diese Verbindungen mit terminalen Olefinen, einem Oxidationsmittel und einem Palladiumsulfoxid-Katalysator umsetzen und so eine Vielzahl tertiärer Amine mit verschiedenen funktionellen Gruppen erzeugen (siehe Beispiel). Die Chemiker nutzten die Reaktion, um die Antipsychotika Abilify und Semap herzustellen und um bereits existierende Medikamente, die sekundäre Amine sind, wie das Antidepressivum Prozac, in tertiäre Amine umzuwandeln. Dies demonstriert, wie Chemiker aus bestehenden Medikamenten neue herstellen können (Science 2022, DOI: 10.1126/science.abn8382).
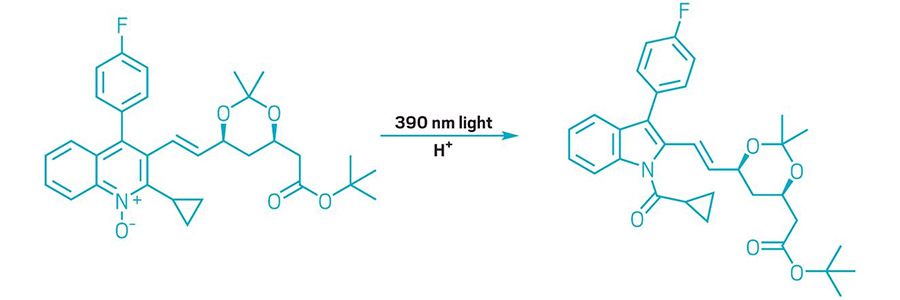
AZAARENES UNTERZOGEN EINE KOHLENSTOFFKONTRAKTION
Das Schema zeigt die Umwandlung eines Chinolin-N-oxids in ein N-Acylindol.
In diesem Jahr erweiterten Chemiker das Repertoire an molekularen Editierungsmethoden, also Reaktionen, die Veränderungen an den Kernen komplexer Moleküle bewirken. So entwickelten Forscher beispielsweise eine Transformation, bei der mithilfe von Licht und Säure ein einzelnes Kohlenstoffatom aus sechsgliedrigen Azaarenen in Chinolin-N-oxiden abgespalten wird, um N-Acylindole mit fünfgliedrigen Ringen zu erzeugen (siehe Beispiel). Die von Chemikern der Arbeitsgruppe um Mark D. Levin an der Universität Chicago entwickelte Reaktion basiert auf einer Reaktion mit einer Quecksilberdampflampe, die Licht verschiedener Wellenlängen emittiert. Levin und seine Kollegen stellten fest, dass die Verwendung einer Leuchtdiode mit einer Wellenlänge von 390 nm eine bessere Kontrolle ermöglichte und die Reaktion auf Chinolin-N-oxide übertragbar machte. Die neue Reaktion bietet Molekülentwicklern eine Möglichkeit, die Kerne komplexer Verbindungen zu modifizieren und könnte Medizinchemikern helfen, ihre Wirkstoffkandidatenbibliotheken zu erweitern (Science 2022, DOI: 10.1126/science.abo4282).
Veröffentlichungsdatum: 19. Dezember 2022

